
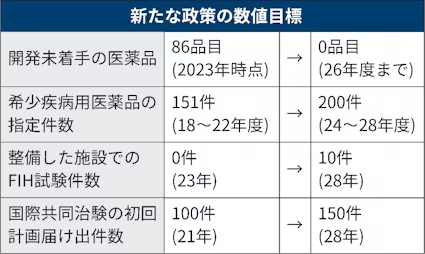
政府は30日、都内で外資の製薬大手を招き「創薬エコシステムサミット」を開催した。画期的な新薬をつくりだすための政策目標と5年間の工程表を示した。
創薬スタートアップへの民間投資額を2028年に2倍にするほか、企業価値が100億円以上の企業を10社以上輩出することなどを掲げた。
会議には米製薬大手のイーライ・リリーやジョンソン・エンド・ジョンソン(J&J)、武田薬品工業など国内外から20ほどの企業・団体を招いた。政府から岸田文雄首相や武見敬三厚生労働相、村井英樹官房副長官らが出席した。
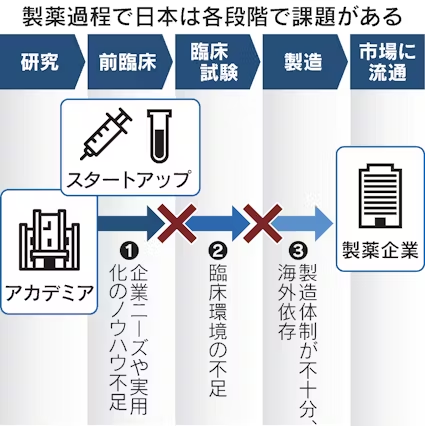
創薬力向上に向けた戦略を策定する背景には、かつて世界有数の創薬国だったにもかかわらず、近年は国際競争力が低下しているとの危機感がある。海外企業との研究開発資金の差や厳しい薬事規制などが影響しているとの見方が強い。

世界の医薬品開発品目数をみると売上高5億ドル以下のベンチャーが8割を占める。米国などではバイオ分野のベンチャー投資が盛んでスタートアップが育つ環境が整う。日本は創薬ベンチャーへの投資額が見劣りする。年間およそ250億円程度で、米国の0.4%にとどまる。
政府が示した工程表には日本医療研究開発機構(AMED)が主に担う政府の創薬ベンチャー支援制度の拡充を盛り込んだ。助成する企業数を現在の11社から28年度に70社まで増やす。
VC(ベンチャーキャピタル)から資金調達したばかりの「アーリーステージ」と呼ばれる段階の企業に助成対象を広げることを検討する。現在はAMEDが認定したVCが10億円以上出資する企業を対象に政府がVC出資額の最大2倍を助成している。
会議に参加した外資製薬による日本のスタートアップやベンチャーへの出資も期待している。
薬事規制の緩和に加え、臨床試験(治験)の体制も整える。3段階の治験のうち一番目にあたる「第1相」で、ヒトに初めて投与する試験(FIH)への支援は創薬力の強化に欠かせない。国際共同治験や専門人材を呼び込むことなどにより23年はゼロだった国内施設でのFIH試験を28年に10件実現すると掲げた。
海外の新薬が日本で使えない「ドラッグロス」の是正についても26年度までに道筋をつける。首相は「世界の創薬基盤の一つとなるべく、日本の創薬基盤の再構築・再強化を図る」と訴えた。
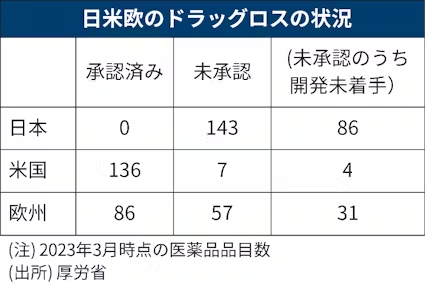
23年時点で米欧で実用化し日本では未承認の医薬品は143品目にのぼる。このうち国内向けの開発に着手していない86品目に関し、26年度までに少なくとも開発に着手するよう企業に要請する。
日本で医薬品を承認審査する医薬品医療機器総合機構(PMDA)は年内に米首都ワシントンで事務所を開設する。日本の薬事制度について情報を発信し、現地の創薬企業に日本への参入を働きかける。
企業側は政府の支援策を歓迎しつつも課題を指摘する意見がある。VCのファストトラックイニシアティブの安西智宏代表パートナーは「臨床試験(治験)拠点や製造体制の整備などは一朝一夕にできるものではない。経験者をどう呼び込むかも課題で、忍耐強く進める必要がある」と語った。
動物向けの抗体医薬品を開発するマブジェネシスの柴崎友一朗執行役員は「スタートアップ側だけでなく事業を見極める力を持ち製薬業界に精通したベンチャーキャピタリストの育成も急務だ」と話した。
バイオ創薬企業の幹部は日本の薬価制度について「国が過度な薬価抑制策をとる限り、米国などと比べて日本市場の魅力は低くなる」と訴えた。

鄭重声明:本文の著作権は原作者に帰属します。記事の転載は情報の伝達のみを目的としており、投資の助言を構成するものではありません。もし侵害行為があれば、すぐにご連絡ください。修正または削除いたします。ありがとうございます。


